PENGERTIAN REAKSI ADISI
Ø Reaksi adisi adalah reaksi penambahan
suatu atom pada ikatan rangkap dalam suatu senyawa. Pada reaksi adisi terjadi
perubahan ikatan, ikatan rangkap tiga, ikatan rangkap dua atau ikatan rangkap
tunggal.
Ø Reaksi adisi adalah reaksi penggabungan
dua atau lebih molekul menjadi sebuah molekul yang lebih besar dengan disertai
berkurangnya ikatan rangkap dari salah satu molekul yang bereaksi akibat adanya
penggabungan. Biasanya satu molekul yang terlibat mempunyai ikatan rangkap.
Contoh reaksi adisi adalah reaksi antara
etena dengan gas klorin membentuk 1,2- dikloroetana.
Dalam reaksi adisi, molekul senyawa yang mempunyai ikatan
rangkap menyerap atom atau gugus atom sehingga ikatan rangkap berubah menjadi
ikatan tunggal.
Alkena dan alkuna dapat mengalami reaksi adisi dengan
hidrogen, halogen maupun asam halida(HX). Untuk alkena atau alkuna, bila jumlah
atom H pada kedua atom C ikatan rangkap berbeda, maka arah adisi ditentukan
oleh kaidah markovnikov, yaitu atom H akan terikat pada atom karbon yang lebih
banyak atom H nya (“yang kaya semakin kaya “). Pada reaksi ini berlaku hukum
markovniknov.
Cara menyatakan konformasi dengan proyeksi Newman
Perhatikan kembali konformer pada etana
Cara menyatakan konformasi dengan proyeksi Newman Dua
konformer etana yang penting: ‘nyaman’ dan ‘gerhana’
Reaksi adisi adalah reaksi senyawa karbon yang melibatkan penggabungan
molekul-molekul. Reaksi adisi juga dapat diartikan sebagai reaksi pemutusan
ikatan rangkap (tak jenuh) menjadi ikatan tunggal (jenuh).
Contoh reaksi substitusi:
Reaksi adisi H2 pada alkena membentuk alkana
H2C = CH2 + H2 --> H3C - CH3
Reaksi adisi H2 pada alkanal
membentuk alkohol primer
Ikatan rangkap C = O pada alkanal bereaksi dengan H2 untuk menghasilkan alkohol primer.
Disebut juga dengan reaksi reduksi karena terjadi
penurunan bilangan oksidasi C
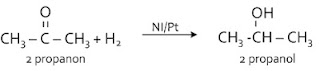
Reaksi adisi H2 pada keton/alkanon
menghasilkan alkohol sekunder
Ikatan rangkap C = O pada alkanon/keton bereaksi
dengan H2 untuk menghasilkan alkohol sekunder.
Reduksi H2O pada asam karboksilat
menghasilkan suatu alkohol sekunder
Ikatan rangkap C = O pada asam karboksilat akan
terbuka akibat penambahan reduktor kuat untuk menghasilkan alkohol primer
dari pembahasan yang di atas, saya masih belum ngerti
tentang permakaian proyeksi newman kapan digunakan? kepada teman mhon
bantuannya. terima kasih.